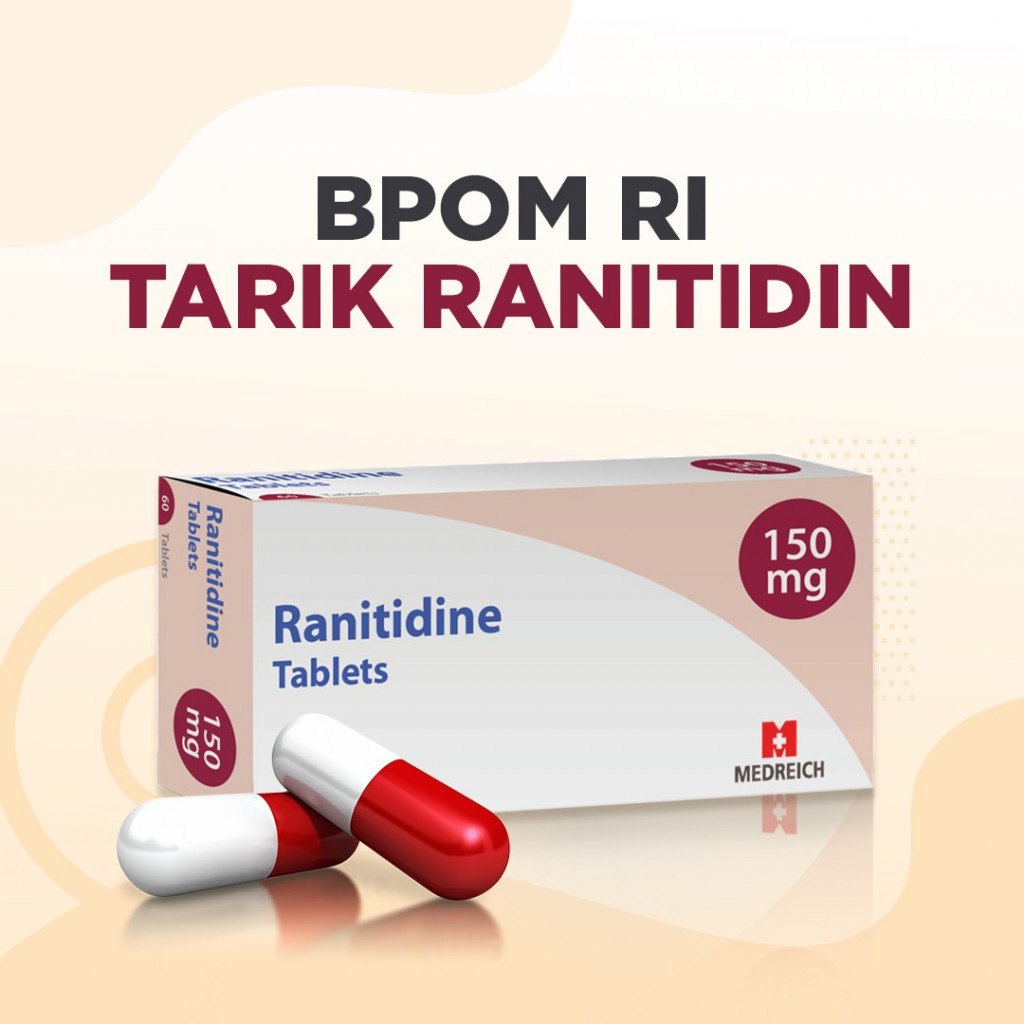
Jakarta: PT Phapros Tbk selaku perusahaan farmasi melakukan penarikan terhadap produk obat Ranitidin. Pasalnya perusahaan tersebut masuk dalam daftar industri farmasi yang wajib menarik obat dari predarannya oleh Badan Pengawas Obat dan Makanan (BPOM).
Corporate Secretary Phapros Zahmilia Akbar mengatakan penarikan telah dilakukan per 25 September 2019. Langkah penarikan ini sebagai tindak cepat untuk melindungi masyarakat dari bahaya ranitidin yang tercemar nitrosodimethylamine (NDMA), senyawa pemicu kanker.
"Penghentian distribusi dan produksi yang dilakukan sejak 25 September sebagai hasil konsultasi kepada BPOM adanya cemaran NDMA," ujarnya melalui keterangan tertulis, Selasa, 8 Oktober 2019.
Saat ini, pihaknya telah melakukan penarikan produk di sejumlah lokasi pendistribusian obat ranitidin mulai dari apotik hingga rumah sakit. Penarikan bakal dilakukan secara bertahap.
Adapun penarikan kembali dilakukan terhadap produk ranitidin HCI cairan injeksi 25 m/ml untuk nomor beta produk jadi yakni 95486160 s/d 190, 06486001 s/d 008, 16486001 s/d 051, 26486001 s/d 019.
"Penarikan menjangkau ke seluruh outlet di seluruh Indonesia seperti, pedangang besar farmasi, instalai farmasi pemerintah, apotik, intalasi rumah sakit, puskesmas, dan dokter," ungkapnya.
Sebelumnya, Badan Pengawas Obat dan Makanan (BPOM) minta lima industri farmasi menghentikan produksi obat Ranitidine. BPOM menemukan cemaran zat nitrosodimenthylamine (NDMA) pada produk Ranitidine.
"Memerintahkan kepada industri farmasi pemegang izin edar produk untuk melakukan penghentian produksi dan distribusi," kata Humas BPOM, Nelly, di Jakarta, Selasa, 8 Oktober 2019.
pada 13 September 2019 US Food and drug administration (US FDA) dan European Medicine Agency (EMA) mengeluarkan peringatan terkait hal ini. Setelah diusut, BPOM menemukan ada lima produsen obat dengan ambang batas cemaran NDMA lebih dari 96 ng/hari.
Jakarta: PT Phapros Tbk selaku perusahaan farmasi melakukan penarikan terhadap produk obat Ranitidin. Pasalnya perusahaan tersebut masuk dalam daftar industri farmasi yang
wajib menarik obat dari predarannya oleh Badan Pengawas Obat dan Makanan (BPOM).
Corporate Secretary Phapros Zahmilia Akbar mengatakan penarikan telah dilakukan per 25 September 2019. Langkah penarikan ini sebagai tindak cepat untuk melindungi masyarakat dari bahaya ranitidin yang tercemar
nitrosodimethylamine (NDMA), senyawa pemicu kanker.
"Penghentian distribusi dan produksi yang dilakukan sejak 25 September sebagai hasil konsultasi kepada BPOM adanya cemaran NDMA," ujarnya melalui keterangan tertulis, Selasa, 8 Oktober 2019.
Saat ini, pihaknya telah melakukan penarikan produk di sejumlah lokasi pendistribusian obat ranitidin mulai dari apotik hingga rumah sakit. Penarikan bakal dilakukan secara bertahap.
Adapun penarikan kembali dilakukan terhadap produk ranitidin HCI cairan injeksi 25 m/ml untuk nomor beta produk jadi yakni 95486160 s/d 190, 06486001 s/d 008, 16486001 s/d 051, 26486001 s/d 019.
"Penarikan menjangkau ke seluruh outlet di seluruh Indonesia seperti, pedangang besar farmasi, instalai farmasi pemerintah, apotik, intalasi rumah sakit, puskesmas, dan dokter," ungkapnya.
Sebelumnya, Badan Pengawas Obat dan Makanan (BPOM) minta lima industri farmasi
menghentikan produksi obat Ranitidine. BPOM menemukan cemaran zat
nitrosodimenthylamine (NDMA) pada produk Ranitidine.
"Memerintahkan kepada industri farmasi pemegang izin edar produk untuk melakukan penghentian produksi dan distribusi," kata Humas BPOM, Nelly, di Jakarta, Selasa, 8 Oktober 2019.
pada 13 September 2019 US Food and drug administration (US FDA) dan European Medicine Agency (EMA) mengeluarkan peringatan terkait hal ini. Setelah diusut, BPOM menemukan ada lima produsen obat dengan ambang batas cemaran NDMA lebih dari 96 ng/hari.
Cek Berita dan Artikel yang lain di
Google News
(BOW)