Otorisasi FDA membatasi antisipasi berminggu-minggu di antara orangtua, yang telah bergumul dengan bagaimana menjalani hidup mereka ketika hanya orang dewasa dalam rumah tangga yang diimunisasi. Ini menghilangkan hambatan bagi pembukaan kembali sekolah dengan mengurangi ancaman penularan di ruang kelas, dan memberi jutaan remaja kesempatan untuk menghadiri perkemahan musim panas, menginap, dan kumpul-kumpul dengan teman-teman.
“Ini adalah berita bagus,” kata Dr. Kristin Oliver, seorang dokter anak dan ahli vaksin di Rumah Sakit Mount Sinai di New York, seperti dikutip The New York Times, Selasa 11 Mei 2021.
“Rasanya kita sudah menunggu lama untuk mulai melindungi anak-anak di kelompok usia ini. Vaksin Pfizer-BioNTech sudah tersedia untuk siapa saja yang berusia di atas 16 tahun,” ujarnya.
Izin FDA bukanlah rintangan terakhir. Komite penasihat dari Pusat Pengendalian dan Pencegahan Penyakit (CDC) diharapkan untuk bertemu segera untuk meninjau data dan membuat rekomendasi untuk penggunaan vaksin pada usia 12 hingga 15 tahun.
Jika panitia mengesahkan vaksin untuk kelompok usia tersebut, seperti yang diharapkan, secara teori imunisasi dapat segera dimulai. Uji klinis telah menunjukkan bahwa anak-anak ini dapat dengan aman menerima dosis yang sudah tersedia untuk orang dewasa.
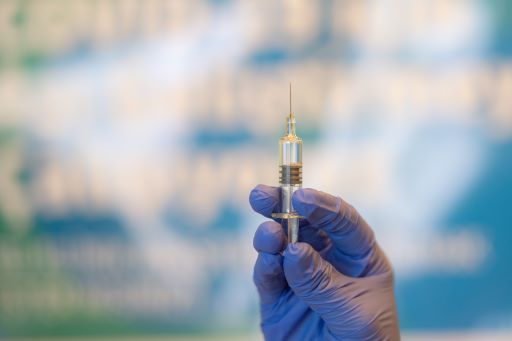
Dalam uji klinis, Pfizer dan BioNTech mendaftarkan 2.260 peserta berusia 12 dan 15 tahun dan memberi mereka dua dosis vaksin atau plasebo dengan jarak tiga minggu. Para peneliti mencatat 18 kasus infeksi virus corona bergejala pada kelompok plasebo, dan tidak ada di antara anak-anak yang menerima vaksin, menunjukkan bahwa vaksin itu sangat efektif dalam mencegah penyakit bergejala.
Vaksin tersebut juga tampaknya aman untuk anak-anak ini, dengan efek samping yang sebanding dengan yang terlihat pada peserta uji coba yang berusia 16 hingga 25 tahun. Demam sedikit lebih umum di antara anak usia 12 sampai 15 tahun yang diinokulasi; sekitar 20 persen dari mereka mengalami demam, dibandingkan dengan 17 persen pada kelompok usia yang lebih tua.
“Tren demam pada usia yang lebih muda konsisten dengan pengamatan dalam percobaan sebelumnya,” kata Dr. Bill Gruber, wakil presiden senior di Pfizer yang juga seorang dokter anak.
“(Vaksin) Kami memiliki keamanan, kami mendapatkan respons kekebalan yang kami inginkan dan kami langsung menunjukkan kemanjuran,” tegas Gruber.
“Sementara perusahaan masih mengumpulkan informasi tentang potensi infeksi tanpa gejala dengan terus menguji peserta uji coba untuk virus corona setiap dua minggu dan memeriksa mereka untuk antibodi yang diproduksi sebagai respons terhadap infeksi alami,” menurut Dr. Gruber.
Dorongan untuk mengimunisasi anak-anak mungkin mengalami masalah yang sama dengan keragu-raguan yang mengganggu upaya untuk menyuntik orang dewasa. Dalam satu jajak pendapat baru-baru ini, lebih dari separuh orang tua mengatakan bahwa mereka cenderung meminta anak-anak mereka mendapatkan vaksin segera setelah mendapat izin.
Dr. Megan Ranney, dokter ruang gawat darurat di Rhode Island Hospital di Providence, mengatakan bahwa dia “tidak memiliki masalah keamanan” tentang vaksin Pfizer-BioNTech. Dirinya mencatat bahwa ratusan juta orang di seluruh dunia telah menerimanya.
Putri Ranney yang berusia 12 tahun sangat ingin divaksinasi, dan putranya yang berusia 9 tahun akan diimunisasi segera setelah dia memenuhi syarat.
“Risiko anak Anda tertular covid-19 dan benar-benar sakit rendah, tapi itu belum nol. Dan risiko mereka sakit atau dirawat di rumah sakit atau lebih buruk dengan covid-19 atau dengan sindrom multi-inflamasi pascacovid lebih tinggi daripada risiko sesuatu yang buruk dari vaksin ini,” ucap Ranney.
Memvaksinasi anak-anak melindungi orang lain di komunitas dari virus, termasuk orang-orang yang tidak dilindungi oleh vaksin, seperti penerima transplantasi organ, pasien kanker, dan mereka yang memiliki respons kekebalan yang terganggu.
“Itu juga melindungi kita semua dari virus yang terus menyebar dan bermutasi lebih jauh,” kata Dr. Ranney.
Pfizer dan BioNTech mulai menguji vaksin pada anak-anak usia 5 hingga 11 tahun pada Maret dan memperpanjang uji coba tersebut bahkan untuk anak-anak yang lebih muda, usia 2 hingga 5 tahun, bulan lalu. Perusahaan selanjutnya berencana untuk menguji anak-anak yang berusia 6 bulan hingga 2 tahun.
Dengan asumsi hasil uji coba menggembirakan, perusahaan berharap untuk mendaftar ke FDA pada September untuk otorisasi darurat untuk memberikan vaksin kepada anak-anak usia 2 hingga 11 tahun.
Hasil dari uji coba vaksin Moderna pada anak usia 12 hingga 17 tahun diharapkan dalam beberapa minggu ke depan. Temuan dari uji coba lain dari perusahaan vaksin pada anak-anak berusia 6 bulan hingga 12 tahun harus tersedia pada paruh kedua tahun ini.
Sedangkan AstraZeneca sedang menguji vaksinnya pada anak-anak berusia 6 bulan ke atas. Johnson & Johnson berencana untuk menunggu hasil dari uji coba pada peserta yang berusia lebih dari 12 tahun sebelum menguji vaksinnya pada anak-anak yang lebih kecil.
Cek Berita dan Artikel yang lain di
Google News