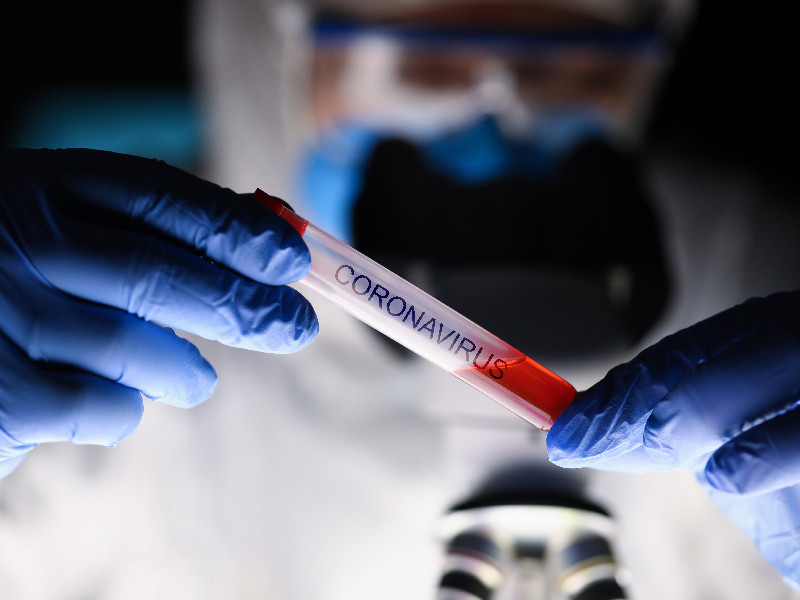
Bandung: Sebanyak 1.620 relawan telah mendapat suntikan pertama vaksin covid-19 buatan Sinovac, Tiongkok, yang dilakukan dalam beberapa sesi uji klinis fase tiga vaksin di Bandung, Jawa Barat.
Direktur Utama Bio Farma, Honesti Basyir, mengatakan pengadaan vaksin covid-19 untuk Indonesia telah ditetapkan oleh pemerintah, yaitu 170 juta jiwa atau sekitar 60 persen dari jumlah penduduk Indonesia.
"Tentu saja hal ini, merupakan program besar, sehingga harus dikelola dengan baik, sejak awal dari mulai uji klinis fase tiga, produksi hingga distribusi dari Bio Farma, mulai tingkat provinsi sampai dengan tingkat puskesmas, termasuk tenaga kesehatan yang memberikan vaksin covid-19 kepada masyarakat," kata Basyir di Bandung, Minggu, 18 Oktober 2020.
Baca: Jalur Pedestarian Lingkar Kebun Raya Bogor Kembali Dibuka
Dia menjelaskan Indonesia memerlukan vaksin covid-19 sebanyak 340 juta dosis dalam waktu setahun. Menurutnya program vaksinasi ini harus dikawal sebaik mungkin oleh seluruh pemangku kepentingan sehingga sesuai prosedur.
Beberapa waktu lalu pihaknya dan Badan POM melakukan inspeksi ke beberapa site uji klinis fase tiga vaksin tersebut di Bandung.
Sementara Direktur Registrasi Obat Badan POM, Riska Andalusia, memberikan apresiasi kepada tim peneliti uji klinis fase tiga dan tim Bio Farma yang sudah menjalankan uji klinis fase tiga sesuai dengan rencana dan jadwal yang ketat.
"Badan POM sebagai regulator memiliki fungsi tidak hanya melakukan fungsi pengawasan, tetapi kami juga berupaya untuk melakukan pendampingan, seperti inspeksi pada hari ini. Kami berharap juga uji klinis fase tiga ini, dilaksanakan sesuai dengan prinsip Cara Uji Klinis yang Baik (CUKB) dan validitas data dapat dipertanggungjawabkan," ungkap Riska.
Ia menambahkan sampai hari ini tidak ada laporan Kejadian Ikutan Pasca Imunisasi (KIPI) atau efek samping yang berat atau serius di antara relawan-relawan vaksin covid-19.
Menurutnya hasil dari uji klinis dapat menjadi data pendukung Badan POM saat mengeluarkan Emergency Use Authorization (EUA) untuk vaksin covid-19 yang akan diajukan oleh Bio Farma pada saat uji klinis fase tiga berakhir.
Nantinya hasil uji klinis fase tiga itu akan digabungkan dengan hasil uji klinis fase tiga di negara lain, seperti Brazil, Chile, Turki dan Bangladesh.
"Uji klinis fase tiga ini dilakukan 'multicenter study' atau dilakukan di banyak tempat. Hal ini berarti uji klinis tidak hanya dilakukan di Indonesia saja, tetapi juga di empat negara lainnya, yaitu Brazil, Chile, Turki, dan Bangladesh," ungkapnya.
Hasil setiap uji klinis di lima negara tersebut akan digabungkan dan dijadikan dasar pemberian izin untuk memproduksi vaksin covid-19 pada masa mendatang.
Setelah uji klinis fase tiga selesai vaksin covid-19 diproduksi oleh Bio Farma, sedangkan dalam proses produksi harus memenuhi aspek mutu. Bio Farma tetap di bawah pengawasan Badan POM untuk pemenuhan peraturan cara pembuatan obat yang baik.
"Tiga aspek tadi, khasiat, keamanan, dan mutu harus dipenuhi oleh Bio Farma, sebagai pendaftar vaksin covid-19 untuk nanti dinyatakan layak atau tidak oleh Badan POM untuk diproduksi hingga distribusi," ujarnya.
Bandung: Sebanyak 1.620 relawan telah mendapat suntikan pertama
vaksin covid-19 buatan Sinovac, Tiongkok, yang dilakukan dalam beberapa sesi uji klinis fase tiga vaksin di Bandung, Jawa Barat.
Direktur Utama Bio Farma, Honesti Basyir, mengatakan pengadaan vaksin covid-19 untuk Indonesia telah ditetapkan oleh pemerintah, yaitu 170 juta jiwa atau sekitar 60 persen dari jumlah penduduk Indonesia.
"Tentu saja hal ini, merupakan program besar, sehingga harus dikelola dengan baik, sejak awal dari mulai uji klinis fase tiga, produksi hingga distribusi dari Bio Farma, mulai tingkat provinsi sampai dengan tingkat puskesmas, termasuk tenaga kesehatan yang memberikan vaksin covid-19 kepada masyarakat," kata Basyir di Bandung, Minggu, 18 Oktober 2020.
Baca:
Jalur Pedestarian Lingkar Kebun Raya Bogor Kembali Dibuka
Dia menjelaskan Indonesia memerlukan vaksin covid-19 sebanyak 340 juta dosis dalam waktu setahun. Menurutnya program vaksinasi ini harus dikawal sebaik mungkin oleh seluruh pemangku kepentingan sehingga sesuai prosedur.
Beberapa waktu lalu pihaknya dan Badan POM melakukan inspeksi ke beberapa site uji klinis fase tiga vaksin tersebut di Bandung.
Sementara Direktur Registrasi Obat Badan POM, Riska Andalusia, memberikan apresiasi kepada tim peneliti uji klinis fase tiga dan tim Bio Farma yang sudah menjalankan uji klinis fase tiga sesuai dengan rencana dan jadwal yang ketat.
"Badan POM sebagai regulator memiliki fungsi tidak hanya melakukan fungsi pengawasan, tetapi kami juga berupaya untuk melakukan pendampingan, seperti inspeksi pada hari ini. Kami berharap juga uji klinis fase tiga ini, dilaksanakan sesuai dengan prinsip Cara Uji Klinis yang Baik (CUKB) dan validitas data dapat dipertanggungjawabkan," ungkap Riska.
Ia menambahkan sampai hari ini tidak ada laporan Kejadian Ikutan Pasca Imunisasi (KIPI) atau efek samping yang berat atau serius di antara relawan-relawan vaksin covid-19.
Menurutnya hasil dari uji klinis dapat menjadi data pendukung Badan POM saat mengeluarkan Emergency Use Authorization (EUA) untuk vaksin covid-19 yang akan diajukan oleh Bio Farma pada saat uji klinis fase tiga berakhir.
Nantinya hasil uji klinis fase tiga itu akan digabungkan dengan hasil uji klinis fase tiga di negara lain, seperti Brazil, Chile, Turki dan Bangladesh.
"Uji klinis fase tiga ini dilakukan 'multicenter study' atau dilakukan di banyak tempat. Hal ini berarti uji klinis tidak hanya dilakukan di Indonesia saja, tetapi juga di empat negara lainnya, yaitu Brazil, Chile, Turki, dan Bangladesh," ungkapnya.
Hasil setiap uji klinis di lima negara tersebut akan digabungkan dan dijadikan dasar pemberian izin untuk memproduksi vaksin covid-19 pada masa mendatang.
Setelah uji klinis fase tiga selesai vaksin covid-19 diproduksi oleh Bio Farma, sedangkan dalam proses produksi harus memenuhi aspek mutu. Bio Farma tetap di bawah pengawasan Badan POM untuk pemenuhan peraturan cara pembuatan obat yang baik.
"Tiga aspek tadi, khasiat, keamanan, dan mutu harus dipenuhi oleh Bio Farma, sebagai pendaftar vaksin covid-19 untuk nanti dinyatakan layak atau tidak oleh Badan POM untuk diproduksi hingga distribusi," ujarnya.
Cek Berita dan Artikel yang lain di
Google News
(DEN)